Atlas de las Plantas de la Medicina Tradicional Mexicana
Atlas de las Plantas de la Medicina Tradicional Mexicana

|
| La imagen fué proporcionada por: Jaime Raúl Bonilla Barbosa CONABIO |
San Luis Potosí: tsokoy k´winim, tsokoy (tenek).
Arbusto de 1.5 hasta 2m de altura, tallos con pelos, tiene las ramas largas. Las hojas están partidas formando tres picos. Las flores son amarillo-cremosas y grandes, sus pétalos se tornan rosados. Sus frutos son cápsulas que al secarse se abren en tres o cinco partes, de las cuales sale una pelusa que es la que conocemos como algodón.
Es originario del Nuevo Mundo; habita en clima cálido desde el nivel del mar hasta los 30msnm. Planta cultivada en huertos familiares, está asociada a bosques tropicales caducifolio, subcaducifolio, subperennifolio y perennifolio.
En Quintana Roo y Tabasco, la enfermedad en la que más se utiliza esta planta es la tos. Para aliviarla se emplea la savia de las hojas diluida en agua y el fruto asado para obtener su jugo, o las semillas en cocimiento o mezclado con maguey morado, hormiguera o hierba de San Nicolás (spp. n/r) para hacer una pócima. También suele ocuparse en el tratamiento de otras enfermedades respiratorias como el asma, gripa, garraspera, catarro, resfriado y acecido (respiración dificultosa que produce en el pecho del enfermo un silbido), en este último caso se soasan las hojas y con el jugo se untan en el pecho.
Incluso, se refiere que esta planta puede ser aprovechada como auxiliar en el parto o en trastornos menstruales, en heridas, llagas, picadura de alacrán o mordedura de víbora y para bajar la presión o la fiebre.
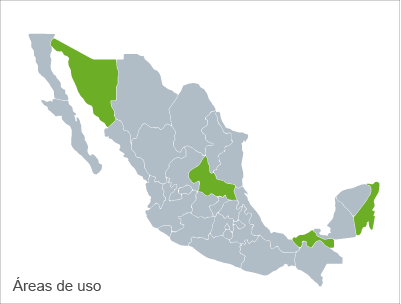
Se menciona su utilidad tanto en el norte, especialmente en Sonora, como en el sur del país.
En el siglo XVI, el Códice Florentino relata que la semilla molida sirve para los postemillas (costra que se crea en las llagas o granos cuando se van secando) y la sarna.
Se conoce bastante bien la química de G. hirsutum. En la semilla se han detectado los carotenos auroxantina, alfa- y beta-caroteno, flavoxantina, gosiverdurín, luteín isoluteín, neocromo, neoxantina, fitoeno, fitoflueno y violaxantín; los triterpenos alfa-amirina, cicioartenol y 24-metilene-cicloartanol; los sesquiterpenos gosifulvín, gosipol, hemi-gosipol y gosipurpurin; el esterol daucosterol; los compuestos fenílicos ácidos para-hidroxi-benzoico, orto y para-cumárico, ferúlico y vainillíco; y los flavonoides, gosipetín, gosipitrín y leuco-definidín. Los brotes contienen un aceite esencial en el que se han aislado los sesquiterpenos alfa-bergamoteno, beta-bisabolol, cariofileno, copaeno, farneseno, farnesol, delta-guaieno, alfa-humulenoy gama-muroleno; los monoterpenos delta-cadineno, alfa-fencheno, l-para-mentén-9-al, mirtenal y mirtenol; los componentes fenílicos acetofenona, benzal-dehído, para-totualdehído y metil-tolil-cetona; y el alcaloide indol. En las partes aéreas de la planta se han identificado los sesquiterpenos ácido abscícico, gama-bisaboleno, beta-cario-fileno, gosipol y éter metilíco de lacimileno C; los esteróles estigmasterol y beta-sitosterol; los flavonoides catequina, epi-catequina y quercetina; los compuestos fenílicos ácidos cafeícos, clorogénico y gálico, y alcaloide del indol indol-3-carboxaldehído.
Se ha demostrado que las brácteas, la flor y los tricomas de G. hirsutum estimulan la síntesis de prostaglandinas y la agregación de plaquetas cuando se probó tanto en cultivo de células, como in vivo en ratas, cuyo y conejo.
Los tricomas provocan la liberación de histamina en rata y la fracción de taninos de las brácteas estimula la proliferación de linfocitos T humanos.
Los extractos acuosos de las flores, raíces y la planta completa indujeron un efecto estimulante del útero de rata y de gato en estado de preñez.
Esta acción estimulante de músculo liso se observó en la rata cuando se administró la semilla como parte de la dieta al 17%.
La semilla provocó un efecto antiespermatogénico y espermicida en rata cuando se administró como parte de la dieta en una proporción del 8%; así como la inhibición de la fertilidad en el mismo animal cuando se administró en un 12.12%, como parte de la dieta. Cuando la harina de la semilla de algodón se extrajo con éter fue inactiva, en cambio las glándulas de pigmento ejercieron también un efecto espermatogénico en la rata, por vía oral a la dosis diaria de 25mg/animal, durante 26 días. Se observó el 100% de espermatozoides muertos. La misma propiedad se describe para el aceite obtenido de la semilla.
La harina obtenida de la semilla adicionada en un 50% en la dieta a ratas provocó la disminución de los niveles de testosterona, androsterona y dihidrotestosterona después de cuatro semanas.
En el hombre, se sospechó que el aceite crudo de la semilla al usarse para cocinar los alimentos provocó una disminición de la velocidad de nacimientos de niños en ciertas áreas de China.
El extracto acuoso de la raíz, indujo la menstruación en una mujer adulta, al ser ingerido oralmente.
El gosipol es el principio tóxico de la semilla de algodón.
Los tricomas y las glándulas del pigmento provocan una acción alergénica en animales de laboratorio y el hombre. Un gran número de investigaciones han comprobado las acciones tóxicas ejercidas por la semilla incluida en la dieta o algunos de sus extractos o fracciones, así como las glándulas de los pigmentos, en diferentes animales de experimentación.
Entre las acciones que se observaron, se indican un incremento de los niveles séricos de lípidos y colesterol, un efecto carcinogénico, hay pérdida de peso, vómito, respiración corta rápida y difícil, anemia y debilidad en los músculos de las piernas.
Las semillas también contienen gosipol por lo que deben presentarse síntomas de envenenamiento similares a los de G. barbadense.
Planta de origen americano cuya aplicación actual como cicatrizante se indica desde el siglo XVI.
CIQRO, CSAT, UAS, UJAT.
Botánica. Gutiérrez E. 1983; López R. e Hinojosa A. 1988; Mata S. 1987; Ortíz G. 1987; Ortíz G. 1990; Pulido T. 1993; Serralta L. 1991.
Ecología. Centro de Investigaciones de Quintana Roo, 1991; Index Kewensis.
Etnobotánica. López R. e Hinojosa A. 1988; Ortíz G. 1987; Ortíz G. 1990; Romero C. 1984.
Historia. Estrada E. 1989 (Códice Florentino. 1548-1582).
Química. Anónimo 1980,1984; Bevardi L. y Goldblatt L. 1980; Chahuar) U. 1984; Elsen G. W. y cols. 1985; Hallon J. y Bell A. 1979; Hedin P. A. y cols. 1975; Hubac C. y cols. 1981; Jones L. 1979; KajimotoG. yShibahara A. 1983; Minyard J. P. y Hedin P. A. 1967; Me Cormíck J. y cols. 1978, 1984; Raj S: 1972; Samkar S. y cols. 1983
Farmacología. Anónimo 1979; Bellamy W. 1866; Greenblatt G. y Elissalde M. 1985; El-Mahdy N.y cols. 1985; Herrera J. y cols 1983;Huang L. 1980; Liu B. S. 1957; Moore L. 1935; Reder R. y Gllup W. 1935; Rohrbach M.y cols. 1982; Satthawongsakul S. 1980;Scout J. 1911; Sotelo A. y cols. 1982; Tso W. y Lee C. 1982; Vuk-Pavlovic Z. y Rohrbach M. 1990; Ziprin L. y cols. 1981, 1981
Principios activos. Morton J. F. 1981.
Toxicidad. Anderson P. y cols. 1982; Cabel C. y Earle I. 1956; Duke J., 1991; Bhaham J. y cols. 1967; Dai R. y cols. 1978; Eagle E. y cols. 1948; El-Nockrashy A. y cols. 1963; Goldberg S. y Maynard L. 1923; Lillie R. y Bird H. 1950; Undsey T. y cols. 1980; Lyman C. y cols. 1963; Menaul P. 1922; Tone J. y Jensen D. 1970; Withers W. y Carruth F. 1913, 1918.